No.2 Caspase と細胞死が繋がった1990 年代
三浦 正幸 東京大学薬学部遺伝学教室
【細胞死研究以前】
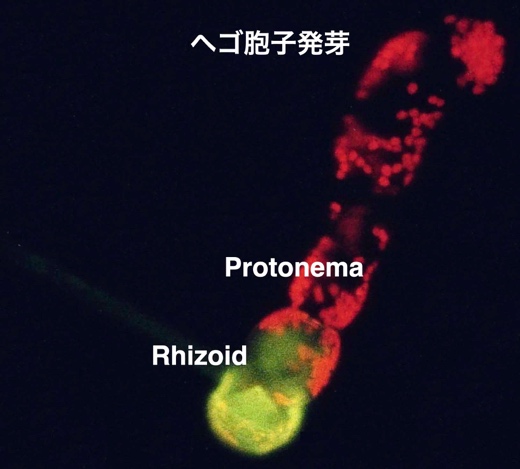
私は東京都立大学の卒業研究から修士まで自分勝手にシダ植物胞子の発芽(仮根と原糸体細胞の分化)時の遺伝発現変化を追っていました。この胞子発芽はフィトクロム依存で発芽の同期が光で制御できます。分化前後の状態が揃った綺麗な細胞集団を扱うことができる訳です。実験デザインは勿論、材料集め(胞子が沢山取れる数メートルもある木生シダ(ヘゴ)を求めて、熱川のバナナワニ園とか東大小石川植物園へ行ってもらってきました)、2次元電気泳動槽作り、船便での論文自費投と、なんでも周りの人に聞きながら一人でやっていました。同じ代謝生理学教室の小柴共一先生は見境のない議論が好きで、そこに集まった同期の八木健さん(現阪大)、戸村秀明さん(現明治大)といくらでも研究の話をしました。

シダ胞子発芽の研究は気にいっていたのですが、なにせ我流の研究には限界があります。私は大学に入る前から発生に興味があってその中でも細胞運命の決定がどんな仕組みでなされるかを知りたいと思っていました。阪大蛋白研で教授になりたての御子柴克彦先生の教室で、博士学生の一期生としてマウス中枢神経系グリア細胞の分化に関係する遺伝子の転写制御を研究しました。御子柴先生は直観力がすさまじく、そこに惹かれて個性豊かな研究者が集まってきて研究室は梁山泊のようでした(岡野栄之先生、田村隆明先生、池中一裕先生、古市貞一先生、宮脇敦史先生など)。このメンバーに囲まれて阪大と、途中から御子柴先生が兼任となった基生研で思いっきり研究ができました。
【細胞死研究との出会い】
慶應大学医学部生理学教室で助手をやっているときに教授の植村慶一先生に留学のチャンスをいただき、1990 年から細胞運命決定を研究している研究室に手紙を書いて留学先を探っていました。神経細胞の分化や、神経系の約8割がプログラム細胞死をおこして失われる線虫を用いた研究をしているマサチューセッツ工科大学(MIT)のRobert H. Horvitz 先生の研究室は非常に魅力的な候補でした。なんの面識もない私からの手紙に対してすぐに丁寧に返事をくださり、自分の研究室で受け入れはできないけれど、プログラム細胞死をやっている研究仲間が同じボストンエリアのMassachusetts General Hospital に研究室をもつことになっているから彼女に可能性を聞いてみるといい、とアドバイスをくださいました。これがJunying Yuan 先生を知るきっかけでした。ちなみにこのとき留学の打診をした線虫研究者は、Horvitz 先生の他に、Martin Chalfie 先生、Cynthia Keynon 先生でした。Horvitz 先生、Chalfie先生はその後ノーベル賞をとっているので、Keynon 先生もとるかも知れません。
さて、Yuan 先生を紹介いただいたのですが調べても殆ど論文が見当たりません。細胞死実行に関わるced-3、ced-4 変異体同定の論文がHorvitz 研からCell 誌に発表され(Ellis and Horvitz, Cell 44, 817-829, 1986)、これら遺伝子の作用をモザイク法によって解析したのがYuan 先生で、ced-3, ced-4 はともに死んでいく細胞で自律的に働く遺伝子だということを示しまた(Yuan and Horvitz, Dev Biol 138, 33-41, 1990)。この論文は玄人受けのする専門的なものだったため、不覚ながらYuan先生に手紙を書くまでその論文を知りませんでした。しかし返事が来て、Yuan 先生は、既にced-3, ced-4 のクローニングに成功していているという事を知り、俄然彼女の研究に興味を持ちました。私のバックグラウンドが哺乳類の分子神経生物学にあったことも幸いしたのかすぐに受け入れる返事を頂きました。1992 年6 月に渡米。アメリカは初めてで、海外の研究室を見たこともなく、ボストンのネイビーヤードにあるMassachusetts General Hospital(MGH)-East になんとかたどり着いてYuan 研はどこかと聞いた実験中の女性がYuan 先生その人でした。私の英語は本当にひどくて会話にならず、Yuan 先生は私も上海からボストンに来た時はそうだったと言って、時間をかけて会話につきあってくださり、英語と漢字の混ざった筆談で留学初日が終わりました。ZOOM 面接をしたら間違いなく却下されたところです。
【Yuan 先生のこと】
JCB にYuan 先生のインタビュー記事(JCB 178, 174-175, 2007)がでていますので、その内容も含めYuan 先生の経歴と人となりを紹介します。公表された論文が一つあるかないかの時にハーバード大学/MGH でPI ポジションを得たとは驚きですが、論文発表前の研究の質と量を見れば当然とうなずけます。目利きがいて、論文数に関係なく研究内容と人物を評価した人事は素晴らしかったといえます。Yuan 先生は上海生まれ。10代までは文化大革命の真っ只中で、将来は農業か工場で働くかくらいしか選択肢はなかったといいます。農作業も結構やったとのことで、作物の種なんかよく知っています。文化大革命が1976 年に終わり1977 年にNational Higher Education Entrance Examination が行われ高等教育に進むチャンスがきました。10 万人以上が受けた試験でYuan 先生は一位となり、上海の復旦大学で学んで1982 年に生化学の学士を取得します。そして再びチャンスが訪れます。China-U.S. Biochemistry Examination and Application (CUSBEA) program の募集が行われたのです。Yuan 先生は25000 人が応募した中の2 位でプログラムに採用され、ハーバード大学に大学院生として入学しました。Yuan 先生は優秀な中国人がアメリカの大学院に進学した第一世代といえます。大学院のコースでハンチントン病の患者に接し、神経変性疾患の発症機構に興味を持ったそうです。また、神経発生のコースでRonald W. Oppenheim 先生(神経発生学者でViktor Hamburger 先生の弟子。Hamburger 先生はNGF を発見したLevi-Rita Montalcini 先生の米国での指導者でもある)が、発生では50%もの神経が死んでいくことを話し、神経細胞死に興味を持ちました。しかしハーバードには細胞死の基本的な仕組みを研究している研究室はなく、どうしたものかと思っていたところでHorvitz 先生のセミナーで線虫のプログラム細胞死の話を聞きます。線虫では131 個の細胞が発生で死んでいきますが、そのうち105 個は神経系の細胞です。これだ、ということで細胞が死んでいく仕組みを研究テーマにするためにハーバード大学に籍を置きながら、研究はMIT のHorvitz 研究室で行いました。そこで線虫の細胞系譜をひたすら観察する遺伝的モザイク解析と、トランスポゾンを用いた遺伝子クローニングの研究を主導し、ced-3, ced-4 遺伝子が細胞自律的に細胞死を実行する事、そしてそれら遺伝子クローニングを成功させました。1989 年にハーバード大学のNeuroscience コースでPh.D を取得しています。
Yuan 先生は面白い研究への感受性が素直です。4月1日発行のNature 誌の細胞死と不老に関するジョーク記事(Nature 362, 411, 1993: Dorian Gray mice)に、私はすっかり騙されて、これはすごいことだとラボメンバーに言って回りました。そのとき記事を真に受けてすぐ図書館に文献を探しに走ったのはYuan 先生と私の二人だけでした。Yuan 先生は議論ですぐに盛り上がります。その一方で、研究が始まるとその展開ロジックは非常に明快です。直観から入る興味の広いところと、研究展開の隙のない進め方のコントラストが面白いです。研究以外にもYuan 先生はラボメンバーのことをよく気遣ってくださいました。私が帰国してまもなくあった1995 年1 月17 日阪神淡路大震災の時はすぐに安否を気遣って電話をかけてくださいました。2011 年3 月11日の東日本大震災のときも、放射能の心配や、できる事はないか、との連絡をいただきました。Yuan 先生からは研究のみならず様々なことを教えていただきました。Yuan先生は日本の文化が好きで、京都の古い街並を好み、生け花もします。大の温泉ファンでもあります。そしてもう一つ。人生で一番大事なことはunpredictable に決まる、とYuan 先生はいいます。米国での研究が始まったのもまさにそのようなunpredictable なチャンスをものにした強烈な経験があったからだと思います。
【CED-3 とICE】
私がYuan 研究室で始めた仕事は3つありました。一つはICE/CED-3 ファミリーの機能を調べる実験。もう一つはそれら遺伝子のノックアウトマウス作成。3つ目はICE/CED-3 ファミリーの生理機能の研究です。
1:ICE/CED-3 ファミリーの機能解析
ced-3 遺伝子がYuan 先生によってクローニングされた時点では、この分子がどのような機能を持つのかは全くわかりませんでした。線虫の細胞死研究とは関係なく、複数の製薬企業が炎症に関わるサイトカインIL-1bを成熟・分泌させるプロテアーゼ、インターロイキン1b変換酵素 (IL-1b converting enzyme: ICE)を探し求め、このクローニングに最初に成功したのはImmunex(1992 年4 月2 日のScience 256, 97-100, 1992)とMerck(1992 年4 月30 日のNature 356, 768-774, 1992)でした。ICE は基質の切断部位P1 にアスパラギン酸を要求するこれまでにないタイプのシステインプロテアーゼでした。1992 年4 月27 日にYuan 先生とced-3 の仕事をしていたShai Shaham 先生(現Rockefeller 大学)がBLAST をかけCED-3 protein と初めてホモロジーのあるタンパク質がヒットしてそれがhuman ICE でした (Horvitz, Bioscience Reports, 23, 239-303, 2003)。Yuan 先生は、私が6月にYuan 研に参加する直前にスーパーテクニシャンのHong Zhu さんとhuman ICE cDNA をプローブとしてlow stringency hybridizationによってマウス胸腺cDNA ライブラリースクリーニングを行っていて、私が参加した時にはいくつかポジクローンが取れていました。そこですぐに始めたのはICE が細胞死遺伝子として機能するかを調べる実験でした。遺伝子の機能を調べるときには目的としている遺伝子を細胞で過剰発現させて調べますが、これが細胞死遺伝子の場合、安定した発現細胞株を作って調べるわけにはいかず、ちょっとした工夫が必要でした。細胞死遺伝子にレポーターをつけることによって一過性発現でその発現細胞がどう変化するかを追うことができるはずです。そこでICE あるいはced-3 にレポーター遺伝子であるlacZ(b-ガラクトシダーゼ)をつけた融合遺伝子を培養細胞Rat-1 に導入しました。期待に胸を踊らせてtransfection した翌日、レポーター遺伝子の発現を見たときの印象的な顕微鏡像は忘れられません。X-Gal によって染め出された青い細胞のことごとくが凝縮し、アポトーシスを起こしている様を呈していたのです。すぐにYuan 先生を呼んで顕微鏡を覗いてもらい、So exciting!ということで握手をして喜びました。御子柴研時代にb-ガラクトシダーゼをレポーターにしたグリア細胞遺伝子(myelin basicprotein: MBP とglial fibrillary acidic protein: GFAP)のプロモーターアッセイをひたすらやっていた経験が染み付いていて、promoter + lacZ がICE/CED-3-lacZ fusionに代わっただけのアッセイ系でしたがこれが細胞死研究に役立ちました。
このlacZ アッセイ系でICE を介したアポトーシスが線虫でのced-3 を介したアポトーシスと同様に進化的に保存された遺伝学的カスケードの中で動いていることが判りました。つまり細胞死を実行する遺伝子としてはICE ファミリー遺伝子が、またそれら遺伝子の作用を抑えるBcl-2 ファミリー遺伝子が、それぞれ線虫のced-3、ced-9 に相当する遺伝子として哺乳類で機能しているというアウトラインが明らかになりました。これらの結果をまとめてボストンの隣町、ケンブリッジ市のハーバードスクエアーにあるCell オフィスに自分で投稿論文をもっていきました。”50 Church Street”学生街カフェの一角。ここがCell のオフィスかと身の引き締まる思いでドアをたたきsubmitしたい旨を告げたところTake it easy! と軽く流されてしまいました。相当肩に力が入っていたのでしょう。幸いにもアクセプトの電話をもらいました。脇で聞いていた テクニシャンのHong Zhu さんがReally?と言うのを真に受けてYuan 先生がCell のオフィスに本当かと思わずcall back したのも懐かしい出来事です。これがYuan 研が発足して初めての論文となりました。Yuan 先生が第一著者として線虫のced-3 クローニングをした論文と、ICE/CED-3 機能解析の私の論文はback to back で1993 年11 月19 日に発表されました (Yuan et al., Cell 75, 641-652, 1993; Miura et al., Cell 75,653-660, 1993)。当時Cell はindividual subscription が$105/year という信じられないくらい安い値段でした。月2冊のペースで雑誌がアパートに送られてくるので、寝る前に違う分野の論文を眺めるのが楽しみでしたが、自分の論文が載った号を手にした時はさすがに嬉しかった。
論文がでる一月前、1993 年10 月にボストン近郊、ケープコットのChatham という小さな街で細胞死の国際研究集会”Cell death in cancer and development”がありました。細胞死実行遺伝子の実体が発表されるかもしれないという事で注目された研究会でHorvitz 先生がYuan 先生のced-3 クローニングに関する研究を発表しました。細胞死遺伝子の実態がタンパク質分解酵素という具体的な機能分子として科学者の目の前に現れた瞬間でした。発表後、何人かが会場の電話機に駆けつけたのが印象に残りました。アポトーシス研究が最も熱を帯びた時に、Yuan 先生とともに細胞死遺伝子研究の源流で仕事ができたのは私にとってかけがいのない出来事でした。
データベースサーチからYuan 研ではIch-1 (ICE and CED-3 Homolog-1)/Nedd2(caspase-2)を得てLin Wang さんと上記のlacZ アッセイ系で解析をしました(Wang etal., Cell 78, 739-750, 1994)。Nedd2はSharad Kumar先生(現Univ. South Australia)が筑波理研の野田亮先生の研究室で行なっていた、マウス発生中の脳で発現低下するcDNA をサブトラクション法でとってくる研究から得られていたものです(Kumar et al.,BBRC 185, 1155-1161, 1992)。このとき発表されたNedd2 遺伝子情報のORF は活性中心を含まないものだったのですが、ヒトの胎児脳cDNA ライブラリーから相同遺伝子を取ってくると活性中心も見つかり新たなICE ファミリーであることがわかりました。Kumar 先生もICE ファミリーとしてNedd2 を発表しました(Kumar et al., Genes Dev8, 1613-1626, 1994)。Kumar 先生とはその後、ショウジョウバエのアポトーシス研究でも同じ遺伝子を追いかける良きライバルで友人になりました。
ICE、Ich-1 に続いて、同じスクリーニングで取れた他のファミリー分子をIch-2(caspase-11)と命名してSuyue Wang さんと解析していたのですが、その途中でIch-2/Tx/IcerelII が発表されたため名称の変更を余儀なくされました。この時期、1996 年まではカスパーゼファミリー探しが主としてデータベースを基に活発に行われ、1995年JBC 270 巻の6 月と8 月に同じ遺伝子なのに異なった名前がついた論文が掲載されたり(caspase-4 で統一されたIch-2(pp.15250)/IcerelII(pp.15870)/Tx(pp.18715))、他にもcaspase-3 はCPP32/Yama/Apopain、caspase-8 はFLICE/MACHa/Mch5 と異なる名前で呼ばれるといった状況になりかなりの混乱が生じました。Yuan 研でとったIch-2 を発表した時には名前がIch-3(後のcaspase-11)ということになってしまいました(Wanget al., JBC 271, 20580-20587, 1996)。この混乱した状況を改善するために、1996 年にはこの新しいプロテアーゼファミリーをcaspase として発表順に通し番号をつけて命名するという取り決めがなされました(Alnemri et al., Cell 87, 171, 1996)。C はシステインプロテアーゼ、aspase はP1 にアスパラギン酸を要求するというこのファミリーの特徴を示したものです。私より半年ほど後にYuan 研に参加した森島信裕さん(現理研)はcaspase-12 を担当し、これまでのcaspase とは異なる性質を見出していました。そして中川敏幸さん(現岐阜大学)がcaspase-12 の研究を引き継いでノックアウトマウスを作成し、ER stress に耐性を示す表現型を見出しました(Nakagawa et al.,Nature 403, 98-103, 2000)。
今にして思うとYuan 研でとったcaspase family はどれもアポトーシス誘導機能としては癖のあるものでした。caspase-1 は基質であるGasdermin D を切断することによるpyroptosis 実行に特化したcaspase であるとの捉え方が一般的になっています。しかし須田貴司先生(金沢大学)の研究室の仕事でGasdermin D を発現していない神経細胞などではcaspase-1 がBid を切断することによって内因性経路のアポトーシスを実行することが明らかにされました(Tsuchiya et al., Nature Comm.10, 2091, 2019)。私の使ったRat-1 線維芽細胞はGasdermin D を発現していなかったのでしょう。ICE の過剰発現によってpyroptosis 誘導がおきなかったことがアポトーシス研究に幸いしました。
プロテアーゼを過剰発現したらICE でなくても細胞死が誘導されるとは予想される懸念ですが、細胞内プロテアーゼはそれほど無節操に働くものではありません。プロフォームはあまり活性を持たず、何らかの活性化プロセスを必要とします。しかしICE の過剰発現実験をしていた当初からこのことは気になっていました。プロテアーゼとは関係のないBcl-2 でICE による細胞死が抑制されたことでアポトーシス経路に依存した細胞死であることが判りホッとしたのを覚えています。caspase-1 が開始caspase であったことも過剰発現による活性化を容易にしていました。その後同定された細胞死実行caspase であるcaspase-3 はそれだけの発現では活性化が困難です。Yama(ヒンズー語の死神を意味する)/caspase-3 を同定したDixit 研は、その機能アッセイでprocaspase-3 には活性がなく、ICE によってYama が活性化されることを示しています(Tewari et al., Cell 81, 801-809, 1995)。単純なRat-1 細胞でのICE 過剰発現実験でしたが、様々な要因が重なってICE によるアポトーシス誘導を可能にしていたのです。
Alnemri 研(Thomas Jefferson Univ)はCPP32 としてcaspase-3 を報告(Fernandes-Alnemriet al., JBC 269, 30761-30764, 1994)しましたが、baculovirus を用いた昆虫Sf9 細胞での強力な過剰発現ではICE と同様にCPP32 のアポトーシス誘導を見ています。この場合はウイルス感染による細胞ストレスが開始カスパーゼを活性化したのかもしれません。
1995 年7 月に初めて“Cell Death”のGordon Conference がありました。
Horvitz 先生、Yuan 先生、長田先生、Dixit 先生、Wyllie 先生がいます。
2:ICE/CED-3 ファミリーのノックアウトマウス
1992 年当時はES 細胞を使ったノックアウトマウスの作成は難しいテクニックで、世界でも限られた研究室だけがその技術を持っていました。MIT のRudolf Jaenisch 先生の研究室はそのような研究室の一つで、彼の研究室ではEn Li 先生が樹立した129S4/SvJae マウス系統由来のJ1 ES 株でDNA methyltransferase 遺伝子のノックアウトマウス作成が行われ (En Li et al., Cell 69, 915-926, 1992)、その後En Li 先生はDNA methyltransferase 遺伝子のゲノムインプリンティング遺伝子発現への役割を明らかにしました(En Li et al., Nature 366, 362-365, 1993)。私がYuan 研に参加してまもなく、En Li 先生がYuan 研のとなりにLab を構えました。すぐに私はEn Li先生に弟子入りしてcaspase-1, caspase-11 のノックアウトマウス作成にとりかかりました。カスパーゼノックアウトマウスを作っていたとき、ES 細胞のスクリーニングはYuan 先生と2人三脚で行いました。

Yuan 先生の出産と重なった時期でもあり、無事出産をした日、ラボの仲間とお祝いにハーバード大学の病院へいくと、開口一番「ES は調子いい?」と質問。さすがでした。そして1週間もたたないうちにラボに出てきたのにも驚きました。caspase-1 KO は3度のES 細胞 screening で2000 くらいのクローンを調べたにもかかわらずノックアウトクローンが得られず、そうしているうちに1995 年にはD3 ES というやはり129/Sv 由来のES 細胞を用いたcaspase-1 KO マウス作成の報告がでました。BASF Bioresearch Co.のグループから2 月に(Li et al., Cell 80, 401-411, 1995)、Richard Flavell 研の杭田慶介先生の仕事 (Kuida et al., Science 267, 2000-2003, 1995)は3月に発表され、ともにLPS 刺激によるIL-1bの分泌がおきずseptic shock に耐性がでるとの結果を報告しました。
一方で、caspase-11 のノックアウトES クローンは比較的すんなりと得られ、表現型解析の途中で私は帰国しました。その後、何度かMGH へ行って実験しましたが、最終的にはSuyue Wang さんが引き継いで、caspase-1 KO と同様にcaspase-11 KO マウスはLPS によるIL-1bの分泌不全、septic shock 耐性がでることを報告しました(Wang et al., Cell 92, 501-509, 1998)。
ところがこれには後日談があります。129 系統のcaspase-11 遺伝子にはエキソン7のスプライシングアクセプターに5ベースの欠損があって、エキソン7がスキップされエキソン8につながりストップコドンが入ること、かつmRNA のnonsense-mediated mRNA decay によってその発現が激減していることがVishva M. Dixit 研 (Genentech)の榧垣伸彦先生によって報告されました(Nature 479, 117-121, 2011)。なんと、私はcaspase-11 にpassenger mutation をもつ129 系統由来のES 細胞にわざわざ遺伝子欠損を入れていたのです。しかし、幸いなことに129 系統のICE 遺伝子は正常なので、LPS によるseptic shock 耐性がでる表現型がcaspase-11 変異によるとの結論は変わりません。
129 由来のES 細胞が初期のKO マウス作成に多く使われたましたが標的遺伝子から10CM の中に平均して20 のpassenger 変異があるとされています。10 世代B6 系統にバッククロスしても標的遺伝子±1CM の領域は91%の確率で129 系統のゲノムDNA を持ち込みます。±10 CM では39%の確率でその領域は129 系統の配列が持ち込まれます。そのためいくつかのpassenger 変異を129 系統から持ち込むことはJ1 やD3 ES を用いたKO では避けられないことをPeter Vandenabeele 先生(Ghent 大学)のグループは報告しています(Vanden Berghe et al., Immunity 43, 200-209, 2015)。pannexin-1 はcaspase-11 と4CM 離れた遺伝子で、ATP などを通過させる細胞膜のチャネルです。pannexin-1 KO マウスはLSP によるseptic shock に耐性があるとの表現型はC57BL/6由来の ES 細胞でKO すると耐性が消えるためcaspase-11 のpassenger mutation によることがわかりました。caspase-1 はcaspase-11 と隣り合わせの遺伝子です。caspase-1 KO マウスのLPS 耐性表現型に関しても、Thirumala-Devi Kanneganti 先生(St. Jude小児研究病院)のグループがゲノム編集技術を用いてC57BL/6 背景でcaspase-1 KO マウスを作ると表現型が消えることとを報告しています(Ming Man et al., Sci Rep 7:45126, 2017)。やはり初期のcaspase-1 KO マウスのLPS によるseptic shock 耐性表現型はcaspase-11 のpassenger mutation によると考えられます。
3:ICE/CED-3 ファミリーの生理機能
ICE の機能解析に有効だったのは牛ポックスウイルス由来のCrmA というセルピンに似たタンパク質です。CrmA がICE 活性を特異的に抑制するとの報告は私がICE の解析を始める直前に発表されました(Ray et al., Cell 69, 597-604, 1992)。ICE の過剰発現でアポトーシスを誘導することはわかったのですが生理的な刺激でのアポトーシスにICE が関わるかどうかを調べたいと思い、HeLa 細胞にTNFa+CHX(シクロヘキシミド)でアポトーシスを誘導する実験にCrmA を用いてICE の関わりを調べました。CrmA は非常によくTNFα+CHX のアポトーシスを抑制することがわかりCrmA が標的とするプロテーアーゼ(当時はICE のみが知られていた)が生理的なアポトーシスに関わることがわかりました(Miura et al., PNAS 92, 8318-8322, 1995)。この論文を投稿している時にDixit 研はMCF7 を用いたTNFaあるいはFas 抗体+CHX アポトーシスの誘導系でやはりCrmA が抑制効果を持つことを発表しました(Tewari and Dixit, JBC 270, 3255-3260, 1995)。1996 年にミュンヘン郊外で行われた細胞死に関する日独シンポジウムに参加した際にApo-1 抗体を見出したPeter H. Krammer 先生(Trauth et al., Science 245, 301-305, 1989)が来ていました。細胞死を誘導するFas 抗体を米原伸先生(京都大学)は細胞死実行経路がほとんどわからない時代に見出し、この現象に注目しました(Yonehara et al., JEM 169, 1747-1756, 1989)が、なんと同じ抗原を認識する抗体を同じ時期にKrammer 先生たちも独立に得ていたのです。科学の大きな発見ではなぜかこのような同期がおこります。このシンポジウムでKrammer 先生はFas/Apo-1 によるアポトーシスはリガンド刺激を受けたFas/Apo-1 の細胞質領域にFLICE/caspase-8 がリクルートされて活性化されることを発表しました。caspase が外因性の細胞死経路の最上流にあったのです。この仕事はDixit 研、Marcus E. Peter 研との共同で行われました(Muzio et al., Cell 85, 817-827, 1996)。同じ号のCell にBack to Back でワイズマン研究所のDavid Wallach 先生はFas 以外にTNFR1 を介したアポトーシス経路の開始にもMACHα/caspase-8 が関わることを示し、CrmA はcaspase-8 も標的にすることを発表しました(Boldin et al., Cell 85, 803-815, 1996)。これらの研究でTNFa,Fas といった外因性アポトーシス経路開始のステップをCrmA は抑制していたことが判りました。ICE/CED-3 の相同分子探索からアポトーシス実行メカニズムの研究に移行した時でしたが、そうなると世界中で行われている様々な研究の断片が一気にいろんなところで繋がってくる大きな研究のうねりを感じました。
その後、長田重一先生(大阪大学、京都大学)のグループによってcaspaseがアポトーシス実行の最終段階に果たす役割が明らかにされました。長田研はアポトーシス実行の鍵となる核DNA断片化に関わるcaspase-activated DNase (CAD)の活性化がCADと結合している阻害タンパク質ICADのcaspase-3の切断によること(Enari et al.,Nature 391, 43-50, 1998)、caspase-3は、フォスファチジルセリン(PS)の細胞外側への露出に関わるスクランブラーゼXkr8を活性化する一方(Suzuki et al., Science341, 403-406, 2013)、細胞の外側へ露出したPSを細胞質側に引き戻すフリッパーゼATP11Cを不活性化すること(Segawa et al., Science 344, 1164-1168, 2014)を明らかにしました。アポトーシス実行の礎石になるそれぞれのステップにcaspaseが絡んでいたとは驚きで、Fas/Fas ligand遺伝子の同定(Itoh et al., Cell 66, 233-243,1991; Suda et al., Cell 75, 1169-1178, 1993)から、eat me signal提示機構までのアポトーシス経路を一気通貫して解明した長田研の研究は圧巻というしかありません。

【おわりとはじまり】
細胞運命がどうやって決まるかに興味をもって細胞死研究を始めましたが、1994年にボストンから帰ってきて細胞死という細胞運命が体の中でどんな働きをしているのかに興味がでてきました。ではどうやってアプローチするか。発生の研究が因果関係を求める還元的な方法論で進んできたことを、Wilhelm Rouxのhot needle experimentを紹介しながら加藤淑裕先生(当時は三菱化成生命科学研究所)が大学院講義で話してくださいました。プログラム細胞死という生命現象を聞いたのも加藤先生の講義でした(写真は都立大学理学部の講義室)。
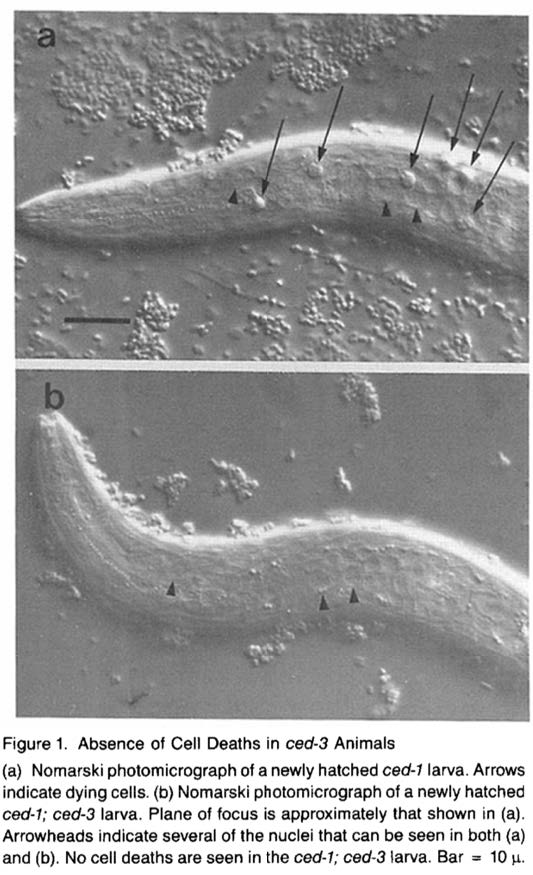
細胞死を知りたければ細胞死をおきなくすれば、その因果がわかるはずです。この方法論は、EllisさんとHorvitz先生がced-3を線虫で同定した時に用いたものです(Ellis and Horvitz, Cell 44,817-829, 1986)。当時、死細胞の貪食がうまくいかない変異体としてced-1が得られていました(Hedgecock et al., Science 220, 1277-1279,1983)。死骸が貪食されずに残るced-1の表現型は細胞死が実行されたからおこる。だったら死骸が生じる原因である細胞死実行が止まれば死骸はできないはずです。そこでced-1変異体にさらに変異を誘導してced-1の表現型(死骸が体に残る)が消えれば、その二重変異体は細胞死実行遺伝子にも変異が入っているはずだと。このスクリーニングで見事ced-3とced-4が得られました(右の写真)。細胞死の仕組みに関しては因果を求める方法論が成功した訳です。
では、アポトーシスの働きは死骸を作る以外にはないのでしょうか。それを知るためには、caspaseの抑制で何が起こるかを詳しく調べればいいはずです。しかしced-3変異体が一見、なんの問題もなく発生することから、アポトーシス阻害の影響を知ることは簡単ではないことが想像できます。線虫では131個の細胞死が、細胞が生まれて2時間以内に何かの働きをする間もなく実行されます。細胞運命を決める重要なced-3遺伝子ですが、個体では何をしているかが明確ではないのです。この頃からずっと、個体でのアポトーシスの働きを知ろうとcaspaseの研究をしていますが、caspaseの機能研究にも増して、アポトーシスの役割を知ろうとすることは確かに手強い。この疑問は、そもそも還元的なアプローチでは解答できない、生き物の捉え方にそのものに関わるものかもしれません。ますます面白くなってきました。
明治の極端な西洋化に対して、日本の伝統的な学芸を捉えなおす動きが活性化されました。明治に生きた岡倉天心(1863-1913)の日本美術復興に関する活躍が面白くていくつか本を読みました。天心は東京美術学校開校に奔走し1890年に29歳で校長に就任するも、日本美術を中心においた天心路線に対して、西洋画、西洋彫刻を推進する欧化派の攻勢があり1898年に辞職に追い込まれました(美校騒動)。志を共にする17人は美校を連袂辞職し、天心とともに日本美術院を立ち上げて日本画の近代化を進めたのです。天心は1905年からボストン美術館の顧問に、1910年には中国・日本美術部長に就任し、晩年まで年の半分はボストンに住んでコレクションの充実と東洋美術の理解を促しました。ボストン美術館(Museum of Fine Arts)はハーバード/MGHのIDで無料だったのでよく行きました。天心の弟子、横山大観や菱田春草は西洋の表現技法を研究し、日本画の決まりごとを破壊(destruction)して新しい表現を創造(creation)しました。横山大観は総長40mにも及ぶ水墨画の代表作「生々流転」を1923年9月1日に院展に発表します。発表前の8月26日に都新聞は「今秋の美術界を震駭さすべき大作」と紹介していました。


発表当日の11時58分、関東大震災が発生。会場にいた横山大観は自ら作品を巻いて持ち出して作品は被害を免れたのです。この「生々流転」は葉の雫が集まって瀬となり、淵となり、大河となって、海に注ぎ、龍巻となって天に上る様を描いたもので、水の一生を東洋の自然観で現したものです。始まりと終わりが境目なく続きます。写真は1906年から天心と大観、春草らが創作に励んだ茨城県五浦(いづら)の日本美術院。現在は茨城大学五浦美術文化研究所として整備されています。六角堂や天心邸が見えます。天心が日本美術にこだわったのは、欧化一辺倒の風潮に対してnational individualityが重要で、歴史で培われた⽂化の独⾃性に重点を置いて、必要なものを外から学びとるべきであるとの考えからでした。研究に関しても知らず知らずに⾝についた歴史性が研究者にはあって、それが研究の個性を創ると感じます。⾃分の場合はlacZアッセイだったのかもしれません。今も⾏なっている細胞死の⽣体イメージングも源流はそこにありそうです。

私たちの体では気づかないうちに1%もの細胞が毎日入れ替わっています。「生々流転」あるいは「生死流転」がさりげなくおきているのです。おわりは、はじまりです。細胞死の働きは一方向の因果を求めてわかるようなことではなくて、時間でうつろう現象を刻々と追うことが求められます。遺伝学に生理学を持ち込まないと太刀打ちできなそうです。
2017年6月にYuan先生が東京に来るというので、これまでの日本人ポスドクが全員集合して、Yuan先生の米国科学アカデミー会員への就任を祝いました。Yuan研は私のいた最初期から国際色豊かな研究室で、連続してポスドクが日本からも参加しています。扱った研究テーマは多岐にわたっています。
著者プロフィール:
1983年東京都立大学理学部生物学科卒業
1988年大阪大学大学院理学研究科博士課程生物化学専攻修了(御子柴研究室)、理学博士
1988年日本学術振興会特別研究員
1989年慶應義塾大学医学部生理学教室助手(植村研究室)
1992年Fogarty International Research FellowとしてMGH留学(Yuan研究室)
1995年筑波大学基礎医学系分子神経生物学講師(岡野研究室)
1997年大阪大学医学部神経機能解剖学助教授(岡野研究室)
2001年理化学研究所脳科学総合研究センター細胞修復機構チームリーダー
2003年東京大学大学院薬学系研究科遺伝学教室教授、現在にいたる。

